Factors and Pathways Modulating Endothelial Cell Senescence in Vascular Aging
Keywords: age-related vascular disease; cellular senescence; endothelial cell; molecular player; putative target; signaling pathway.
細胞衰老是細胞應對 DNA 損傷、氧化應激等亞致死性刺激而進入的生長停滯狀態,通過 p53 及 CDK 抑制劑(如 p16、p21)等信號通路調控。該過程在年輕時對胚胎發育和腫瘤抑制有益,但在老年人群中,衰老細胞的累積會加劇癌癥、心血管疾病等年齡相關性疾病的發生。血管由內膜、中膜和外膜構成,其中內膜的內皮細胞(ECs)直接接觸血流,在維持血管穩態中發揮關鍵作用。機械刺激(如血流紊亂)可誘導內皮細胞衰老,引發 DNA 損傷、活性氧(ROS)升高及促炎因子分泌,導致細胞形態改變(扁平增大)、一氧化氮(NO)生物利用度降低。衰老的內皮細胞通過減少血管密度、增加膠原沉積、降低彈性蛋白合成等,促使血管僵硬、炎癥反應增強,最終推動動脈粥樣硬化、高血壓等血管疾病的發展。鑒于此,韓國仁荷大學醫學院細胞間通訊調控研究中心的研究團隊在International journal of molecular sciences期刊發表了一篇題為“Factors and Pathways Modulating Endothelial Cell Senescence in Vascular Aging”的文章。文章旨在深入探究內皮細胞衰老的分子機制,對于開發針對年齡相關性血管疾病的治療策略具有重要意義。

內皮細胞衰老的特征
衰老的內皮細胞呈現體積增大、形態扁平的經典表型,伴隨多倍體增加、SA-β-Gal 活性升高、端粒縮短,以及 p16、p21 和磷酸化 p38 等經典衰老標志物的激活與纖連蛋白、ICAM-1 和 iNOS 等分子的表達上調(圖 1)。其分泌的衰老相關分泌表型(SASP)具有多樣性。如復制性衰老的 HUVECs 可產生 IL8、IL6 等細胞因子,血流紊亂誘導的衰老 HUVECs 表現為適度 ROS 生成,TNF-α 處理或輻射或阿霉素刺激則分別引發不同的細胞因子或趨化因子表達。
線粒體層面,衰老 HUVECs 的線粒體延長并相互連接,伴隨線粒體分裂關鍵蛋白 FIS1 和 DRP1 的表達下調,而 DRP1 缺失會誘導年輕細胞衰老、自噬受損,其在老年大鼠血管內皮中的表達降低也與自噬功能障礙相關,此外蛋白二硫鍵異構酶 A1 缺失可通過 DRP1 亞磺酰化誘導線粒體碎片化及 ROS 產生,進而促進內皮細胞衰老。
氧化應激是內皮細胞衰老的關鍵驅動因素,其產生的 ROS 不僅來自線粒體呼吸,更主要源于 NADPH 氧化酶(NOX)及溶酶體等其他細胞器,NOX 家族中的 NOX1、NOX2 等亞型可通過誘導氧化損傷促進內皮功能障礙。盡管生理 ROS 維持細胞正常功能,但過量 ROS 會加速端粒縮短并激活衰老信號。
代謝上,衰老內皮細胞表現出糖酵解和氧化磷酸化水平降低的特征,卻依賴谷氨酰胺分解維持存活,抑制該過程可選擇性清除衰老細胞;而功能失調的內皮細胞對氧化磷酸化依賴性增強,其過度激活會加劇 ROS 生成與細胞損傷,高血糖應激則通過代謝重編程推動這一過程。在病理模型與臨床樣本中,衰老內皮細胞廣泛存在于兔動脈損傷、糖尿病大鼠血管及人類動脈粥樣硬化斑塊等組織中,其累積與血管應激、衰老及年齡相關疾病(如動脈粥樣硬化、高血壓)密切相關,單細胞測序及干預實驗進一步證實了其在血管衰老中的病理意義,為相關疾病的防治提供了潛在靶點。

圖1 衰老內皮細胞的特征。
內皮細胞衰老相關的分子作用因子與信號通路
許多分子機制與內皮細胞和血管細胞的衰老相關。以下將描述其中特征最明確的機制,并在圖 2 中進行總結。
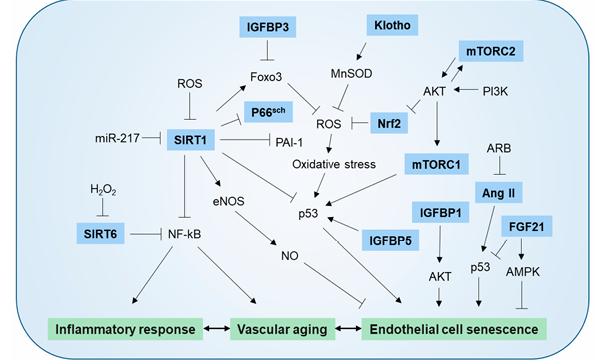
圖2 介導內皮細胞衰老和血管衰老的分子機制。
Sirtuins
Sirtuins 家族中的 SIRT1 和 SIRT6 是調控內皮細胞衰老的關鍵分子。SIRT1 通過 NAD + 依賴的去乙酰化酶活性,維持血管內皮穩態:其可激活 eNOS 促進 NO 生成以抵抗氧化應激,抑制 NF-κB p65 乙酰化來減輕炎癥反應,還能通過 CDK5 磷酸化調控自身核定位,進而影響端粒功能與 p53、PAI-1 等衰老相關因子。最新研究發現,SIRT1 可通過 HERC2 介導的 LKB1 去乙酰化,防止衰老內皮細胞中 LKB1 在核內積累,從而維持血管平滑肌細胞與內皮細胞的通訊平衡。而 SIRT6 作為染色質穩定蛋白,可通過維持端粒功能和抑制 NF-κB 過度激活來延緩內皮細胞衰老,其在糖尿病血管中可減少動脈粥樣硬化斑塊形成,并通過調控 PCSK9-LDL 受體通路降低血脂。兩者通過多通路協同作用,在氧化應激、炎癥反應、代謝調控等層面拮抗內皮細胞衰老,成為血管衰老干預的重要靶點。
Klotho
Klotho 作為一種主要表達于腎臟、少量存在于血管組織的蛋白,在血管衰老調控中扮演關鍵保護角色。動物實驗證實,其可通過上調 NO 生成改善血管舒張功能,同時通過胰島素 / IGF 信號激活 MnSOD 抗氧化酶,減少 H2O2 誘導的內皮細胞凋亡;此外,它還能抑制 caspase 活性、削弱 p53/p21 衰老通路,直接發揮抗內皮衰老作用。臨床研究表明,血漿 Klotho 水平與冠狀動脈疾病、心力衰竭等心血管疾病風險呈負相關,且獨立于傳統危險因素(如血脂異常、高血壓),可作為動脈僵硬度的獨立預測指標。實驗模型中,Klotho 過表達能延緩腎臟與心血管衰老并延長小鼠壽命,而基因敲除則導致血管鈣化等早衰表型。總之,Klotho 通過多機制保護內皮細胞功能,其血漿水平或可成為評估血管衰老及相關疾病的生物標志物,為干預血管衰老提供潛在靶點。
RAAS
腎素 - 血管緊張素 - 醛固酮系統(RAAS)中的 Ang II 是驅動內皮細胞衰老的關鍵因子。Ang II 通過 AT1R 介導 ROS 生成、炎癥反應及 MAPK 通路激活,促進內皮細胞周期阻滯與衰老,其過度激活與動脈粥樣硬化、高血壓等年齡相關血管疾病密切相關,而 AT1R 阻滯劑可拮抗這一過程。在衰老小鼠模型中,Ang II 及其受體 AT1R 表達上調,伴隨 NOX2 及細胞外基質成分增加,而保護性受體 Mas 和 AT2R 表達下降。作為 RAAS 保護性分支的 Ang-(1-7) 可通過作用于 Mas 受體,減少端粒 DNA 損傷、抑制 p53 信號及 SA-β-Gal 活性,從而逆轉 Ang II 誘導的內皮細胞衰老。研究證實,Ang-(1-7)/Mas 軸在調控血管衰老中具有多效性保護作用,不僅拮抗 Ang II 的促衰老效應,還能通過維持 DNA 完整性和抑制炎癥信號,成為干預內皮細胞衰老及相關血管疾病的潛在靶點。
IGFBP
胰島素樣生長因子結合蛋白(IGFBP)家族在調節內皮細胞衰老中呈現復雜作用。IGFBP1 作為家族成員,參與代謝與細胞生長調控,但其同源配體 IGF1 在不同內皮細胞類型中表現出矛盾功能:既能通過激活 IGF1 受體介導輻射誘導的人肺動脈內皮細胞衰老,又能在人主動脈內皮細胞中通過抗氧化應激抑制衰老。IGFBP3 在復制性衰老的內皮細胞中表達上調,其過表達可增強 HUVECs 的衰老表型,而沉默 IGFBP3 則能抑制這一過程。此外,IGFBP5 可通過 p53 依賴性通路誘導 HUVECs 衰老,成為輻射所致內皮細胞衰老的潛在調控因子。
NRF2
核因子 E2 相關因子 2(NRF2)作為氧化應激敏感的轉錄因子,通過結合抗氧化反應元件(AREs)激活抗氧化基因轉錄,在拮抗內皮細胞衰老中起核心作用。激活 NRF2 可抑制細胞衰老,而 NRF2 基因缺失會加速老年腦動脈細胞衰老并增強炎癥反應,同時加劇肥胖等心血管危險因素的不良影響。在非人類靈長類動物和老年大鼠模型中,衰老均導致 NRF2 核轉位障礙及靶基因(如 NQO1、GCLC)表達下降,伴隨線粒體 SOD2 活性降低,進而引發慢性氧化應激。這種 NRF2 功能受損與氧化應激增強的惡性循環,在 H2O2 和高糖等應激條件下尤為明顯,可進一步激活 NF-κB 炎癥通路,推動血管衰老進程。總之,衰老會損害 NRF2 的功能,從而形成一個惡性循環,加劇衰老相關氧化應激誘導的細胞損傷。
mTOR
哺乳動物雷帕霉素靶蛋白(mTOR)作為 PI3K 相關激酶家族成員,通過 mTORC1 和 mTORC2 復合物調控內皮細胞衰老。低劑量雷帕霉素抑制 mTORC1 可延緩 HUVECs 復制性衰老,促進增殖與血管生成,其機制與抑制 S6K 磷酸化及核糖體蛋白 S6 激活相關。熱量限制或雷帕霉素處理可通過降低 mTOR 活性增強衰老小鼠和大鼠的內皮功能,表現為 NO 生成增加及血管舒張能力改善。此外,抑制 PI3K/AKT/mTOR 通路可誘導非經典 SASP 反應,通過自限性炎癥調控維持組織穩態。mTORC2 在衰老內皮細胞中活性升高,沉默 mTORC2 可通過調節 NRF2 減輕氧化應激誘導的衰老。研究揭示 mTOR 信號通路通過整合代謝、氧化應激及炎癥信號,成為內皮細胞衰老的關鍵調控樞紐,其抑制劑(如雷帕霉素)及上下游靶點(如 S6K、NRF2)為干預血管衰老提供了多維度的治療策略。
其他分子
除已闡述的關鍵分子外,諸多其他因子也參與調控內皮細胞衰老。成纖維細胞生長因子 21(FGF21)可通過 AMPK 依賴途徑抑制 p53 激活、誘導線粒體生物合成,從而減輕高糖或血管緊張素 Ⅱ 誘導的內皮損傷與衰老。銜接蛋白 P66shc 通過調節氧化還原代謝,改善衰老內皮細胞對乙酰膽堿的舒張反應。導向受體 UNC5B 則可能通過激活 ROS-p53 通路促進內皮細胞衰老。炎癥因子 IL-17A 可經 NF-κB/p53/RB 信號通路推動內皮衰老,而消退素 E1(RvE1)能通過抑制 pP65、NLRP3 炎癥小體等減輕阿霉素或 IL-1β 誘導的衰老。此外,PPARα 可通過促進衰老相關蛋白 GDF11 的表達抑制內皮衰老,DRG2 缺失會增強 NOX2 介導的 ROS 生成進而促進衰老,CTRP9 能通過 AMPKα/KLF4 通路抑制高血糖誘導的內皮衰老,DPP4 則通過 PAR2-COX-2-TP 軸激活 NLRP3 炎癥小體來誘導內皮細胞衰老。這些分子從代謝調控、氧化應激、炎癥信號等多個維度參與內皮細胞衰老過程,隨著研究的深入,更多相關分子機制將被揭示,為干預血管衰老及相關疾病提供新的思路和靶點。
總之,內皮細胞衰老由端粒縮短、DNA 損傷等多種因素誘導,在血管衰老及動脈粥樣硬化、高血壓等年齡相關血管疾病中起關鍵作用。目前研究已揭示 SIRT1、SIRT6、Klotho 和 NRF2 等分子通過抗氧化應激等機制抑制內皮細胞衰老,而 Ang II、IGFBP3、mTOR 等因子則促進這一過程,其中 Ang II 抑制劑奧美沙坦已顯示出抑制血管炎癥和衰老的作用。未來需在細胞與動物模型中深入解析衰老調控機制,全面挖掘可藥物靶點,并通過鑒定新型標志物和改進檢測技術,提升體內衰老內皮細胞的識別效率。這些研究將為開發針對性干預策略、延緩血管衰老及改善相關疾病預后提供重要理論基礎與實踐方向。
參考文獻:Hwang HJ, Kim N, Herman AB, Gorospe M, Lee JS. Factors and Pathways Modulating Endothelial Cell Senescence in Vascular Aging. Int J Mol Sci. 2022 Sep 4;23(17):10135. doi: 10.3390/ijms231710135. PMID: 36077539; PMCID: PMC9456027.
圖片來源:所有圖片均來源于參考文獻
小編旨在分享、學習、交流生物科學等領域的研究進展。如有侵權或引文不當請聯系小編修正。如有任何的想法以及建議,歡迎聯系小編。感謝各位的瀏覽以及關注!關注“Naturethink”公眾號,了解更多相關內容。
相關產品
免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號



















 采購中心
采購中心